筑波大学 竹越先生に、研究テーマやご自身について語っていただきました
アンバサダーに聞く
アンバサダーに聞く
研究テーマについて
―― 先生の研究テーマについて教えてください。
我々は遺伝子ドーピングの検査法開発に力を入れて研究を進めています。ウマだとJRAでウマの遺伝子ドーピングを研究している方がいますが、ヒトは国内では我々だけと思われます。
―― 遺伝子ドーピングとは何でしょうか?
ドーピングとは、スポーツで運動能力を向上させるために薬物を使用することです。遺伝子ドーピングは、薬物ではなく、例えば筋力を向上するような遺伝子をゲノム編集で細胞に入れ、遺伝子治療の技術を転用して運動能力を向上させることです。運動能力には複数の遺伝子が関係しているようで、どの遺伝子がどのくらいスポーツの成績に関係しているのかは不明です。また遺伝子ドーピングをすることによる体への影響も不明なためリスクが高く、今すぐに遺伝子ドーピングが現実化するとは思えませんが、2018年に世界アンチ・ドーピング機構がゲノム編集による遺伝子ドーピングを禁止リストに追加しましたので注目はされています。
―― 遺伝子ドーピングはどのような方法で検査するのですか?
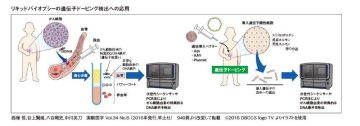
遺伝子ドーピングの検査法としては、本来、遺伝子を発現させた部位、例えば筋肉の筋生検をすればある程度はわかるかもしれませんが、筋肉はアスリートの商売道具なので傷つけるわけにはいきません。アスリートに影響の少ない尿や血液から証拠を拾う手段を選択する必要があります。つまりリキッドバイオプシーです。
例えば肺癌は、後天的に肺だけにある体細胞に遺伝子変異が起きます。今までは開胸もしくは開胸しなくともCT下で肺の癌組織からバイオプシーを行っていました。いずれも侵襲が大きい方法でした。最近は、そんなことをしなくても、ガン組織に特異的だと言われるものが血液の中に出ているということが分かってきたのです、セルフリーDNA(血液中の細胞死によって細胞から放出された遊離DNA)という形で。それを末梢血から同定すれば、肺癌だけに発現している体細胞変異が、リキッドバイオプシーで同定できると知られてきました。そこで思いついたのが、リキッドバイオプシーの遺伝子ドーピング検出への応用です。つまり、競技力のエンハンス目的で後天的に筋肉だけに発現させた遺伝子も、肺癌同様に血中に漏れてくるのではと考えました。
遺伝子検査には、先天性のGermline(生殖細胞系)変異と後天性のSomatic(体細胞系)変異を検査する2種類があります。Germlineは親から先天的に引き継いだ遺伝子変異です。一方、Somatic変異は原則、後天的に発生する変異のため、一代限りで、遺伝しない変異を検査する事になります。遺伝子ドーピングの場合は、治療を目的としない後天的な遺伝子変異導入になりますので、Somatic変異が検出ターゲットとなります。
遺伝子を筋肉などに導入した人は、ドーピングのベクターや外因性遺伝子などがセルフリーDNAのような形で、血中に存在しているのではないかと予想しています。それを検出するために我々は、ベクターとなるアデノウイルスに外来遺伝子を導入して、末梢血のセルフリーDNAを同定する方法を遺伝子ドーピングの検査法として動物実験で検討しています。
―― 検討結果はいかがでしたか?
外来遺伝子としてmCherry遺伝子(翻訳されると赤く光るサンゴの遺伝子)を含むアデノウイルスベクターを作成し、筋肉注射、静脈注射、それぞれで遺伝子導入してみたところ、肝組織と筋肉組織での発現が確認できました。また注射後5日目に、フン、全血を回収して、血球のDNA、血漿のセルフリーDNA、フンのDNAの3種類のサンプルからmCherry遺伝子を含む導入遺伝子をデジタルPCRで検出できることも確認しました。まだ検討課題はありますが遺伝子ドーピングの検査法として使えそうだと考えています。
この研究に関する論文が発表されましたので、詳しくは下記リンクよりご覧ください。
Detection of Transgenes in Gene Delivery Model Mice by Adenoviral Vector Using ddPCR Genes (Basel). 2019 Jun; 10(6): 436.
Takehito Sugasawa , Kai Aoki , Koichi Watanabe , Koki Yanazawa , Tohru Natsume , Tohru Takemasa , Kaori Yamaguchi , Yoshinori Takeuchi , Yasuko Yoshida ,Katsuyuki Tokinoya , Nanami Sekine , Kaoru Takeuchi , Haruna Ueda , Yasushi Kawakami , Satoshi Shimizu , Kazuhiro Takekoshi
https://www.preprints.org/manuscript/201904.0285/v1
The detection of trans gene fragments of hEPO in gene doping model mice by Taqman qPCR assay 2019. PeerJ Preprints7:e27925v1
Aoki K, Sugasawa T, Yanazawa K, Watanabe K, Takemasa T, Takeuchi Y, Aita Y, Yahagi N, Yoshida Y, Kuji T, Sekine N, Takeuchi K, Ueda H, Kawakami Y,Takekoshi K.
今後の展開
―― 今回の検討で遺伝子ドーピングの検出ができそうな感触をつかまれたと思いますが、課題を含めて今後の方向性を教えてください。
今回のマウスのモデル系は、最初の一歩としてはよいのですが、まだまだ解決、発展させていかなくてはならない点があります。本来は血漿からセルフリーDNAが検出できるとよかったのですが、マウスの採血量が少なくて充分に検出できませんでした。抽出法を変えるなどしてチャレンジしたいところです。
また、今回はベクターを使った場合のモデル系です。遺伝子導入法はベクターを使用したものだけではありませんので、他の系でも試してモデルを構築し、遺伝子ドーピングの抑止力になればと思っています。
今回は、予め遺伝子が分かっていて、それを一本釣りするようなストーリーですが、実際の遺伝子ドーピングは不特定の遺伝子がかかわっているので、次世代シークエンサーを用いて底引き網みたいなことをする必要があると思います。しかし次世代シークエンサーを使って全ゲノムを対象にしてしまうと、ゲノム情報がすべてわかってしまいます。本来目的としない遺伝子のことを二次的所見と言うのですが、そういうのが分かってしまうので、次世代シークエンサーを使って未知の遺伝子を同定しようとする場合は、倫理的な側面にも注意していく必要があると思います。
―― 倫理的な側面とはどういうことでしょうか?
それは検査結果の遺伝子情報の取り扱いの事です。日本人は、遺伝を西洋人とは違う感覚で捉えているとよく言われます。日本人には社会的に頻度が高い遺伝性疾患が存在しません。例えば白人だと嚢胞性線維腫、黒人だと鎌状赤血球症という病気があります。それから私もそうなんですけど、初等中等教育において遺伝教育をあまり受けたことはないし、我々は個人主義という考え方になじみがないですよね。人様にご迷惑をかける事とか、人と違う点を異質として恥じるようなところがありますよね。だから遺伝病に対する偏見とか忌避というのはどうしてもあると思います。しかし実際は、変異というのは誰にでも起こることですし、正常な遺伝子を持っている人というのは、誰も存在しないんですよ。特別な人だけではなく、すべての人が取り組まなければならない問題なのです。
まずは遺伝学的検査で知りえた情報が、Germline変異なのかSomatic変異なのかを理解せねばならないし、Germline変異の場合は、本人だけでは済まず、兄弟家族子孫全員が同じ遺伝子を引き継ぐので、ご自身だけでは済まない問題になります。またたとえSomatic変異であってもGermline変異を想起できる所見の場合もあり得ます。遺伝情報の取り扱いを慎重に検討していく必要がありますね。
ドーピングの検査は、断っただけでもドーピング違反になります。ドーピング検査というのは、スポーツの公平性を担保するという大義名分(スポーツの倫理)があるわけですけが、このスポーツの倫理と医の倫理の兼ね合いは、難しい問題を内包しています。技術的には、遺伝子ドーピングの検出ができるようにはなると思いますが、プライバシーに関わる遺伝情報の取り扱いに関しても同時に検討していくことが大切だと思います。私は臨床医と基礎研究の両方に携わっている立場からこの分野の発展に少しでも貢献できたらと思います。
先生ご自身について
―― 先生はなぜ臨床医と研究者の二足のわらじをはくことになったのでしょうか?
恩師に誘われて研究を始めてみて、5年くらい経過したころから非常に面白くなり、止められなくなりました。研究は自分が好きなことができるじゃないですか。音楽家や芸術家など絵を描くみたいなもので、自分で仮説を立てて、人が知らないことをやって、それを発表するというのは、アイデンティティだと思います。
私自身はもともと褐色細胞腫の研究、特に遺伝子診断をメインで続けてきました。ところで、本年の1月に12年かかって、血中遊離メタネフリン測定法という自分の提唱している検査方法が保険収載されたことが良かったです。初めて自分のやったことが、実地臨床で、個人的な経験ではなくて、日本中に還元されて、褐色細胞腫患者さんの福音になるといいと思います。褐色細胞腫の検査は、これまでは蓄尿が必要で、蓄尿の量を正確にするために入院しなければなりませんでした。検査だけのための入院です。一方、血中遊離メタネフリン測定法は採血だけで済む方法なので、検査入院が不要になります。こういう事があると臨床医だけではなく、研究も続けてきてよかったなと思います。
若手研究者へのメッセージ
―― 若手研究者へのメッセージをお願いします。
最近若い人が留学しなくなったことに非常に危機感を持ちます。外に行くというのはすごく大事。日本を外から見る機会というのは、必ずあった方がいいと思います。論文にすぐ結びつかないとしても、全然違う文化圏で半年以上住むというのは、極めて貴重な体験だと思います。私もカルフォルニア大学のサンディエゴ校に留学しましたが、例えば、アメリカって、テレビで毎日見るから隣近所みたいな気がしますが、そのアメリカですら行ってみるると全然違うんですよね。だだっ広いところに住宅だけあるみたいな感じなんです。近所にお店があるという日本の感覚がないんです。ちょっとお腹空いたなと言って、どこかに買いに行こうとする。近所に自動販売機があるわけでもないし、コンビニもないんですよね。家を借りる、電話を引く、それだけでもすごく大変なんです。勉強面もさることながら、住んでみるというのは全然違うので経験したほうが良いと思います。
さらに留学をすると国内だけでなく海外にもネットワーク広がります。留学中に同じラボの仲間だったインドの研究者とは今でも交流があり、彼は最近母国のチェンナイ工科大学で教授になって、先日学振で私のラボに1ヶ月来ていました。学問や英語だけでなく異なる文化に触れられて勉強になりました。今後、彼のラボを含めてインドのラボとのコラボを是非発展させたいです。
また、お医者さんだったら、基礎研究に興味を持って欲しいですね。臨床だけではなくて、基礎的なことにも興味を持つということは、将来臨床に戻っても、モノの見方にも幅が広がりますので、決して損ではないと思います。多少回り道だと思っても、そういうのを経験して面白かったらそれをやって欲しいと思いますね。
今回、コーニングアンバサダーにご応募いただいた時野谷さん
研究室での信頼が高く、今回のアンバサダーへの応募も竹越先生からの推薦で準備から応募までご担当されたそうです。見事アンバサダー認定を勝ち取り研究室の発展にも貢献されました。現在はコーニングアンバサダーの中心人物として積極的に活動されています。研究面でも成果を出されており、今後のご活躍にも期待しています。
筑波大学医学医療系臨床域スポーツ医学・検査医学ホームページ
http://tsukuba-laboratorymedicine.com/
研究室Twitter
@TakekoshiL




